O que é o potencial zeta?
Quase todos os materiais macroscópicos ou particulados em contato com um líquido adquirem uma carga elétrica em sua superfície. Essa carga pode aparecer de várias maneiras - a dissociação de grupos ionogênicos na superfície da partícula e a adsorção diferencial de íons da solução na superfície da partícula. A carga líquida na superfície da partícula afeta a distribuição de íons na sua vizinhança, aumentando a concentração de contraíons junto à superfície. Assim, forma-se uma dupla camada elétrica na interface da partícula com o líquido.
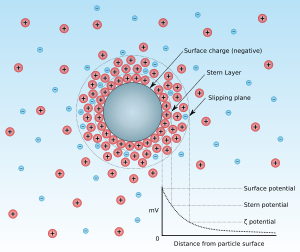
Essa dupla camada divide-se em duas regiões: uma região interna que inclui íons fortemente ligados à superfície e uma região exterior onde a distribuição dos íons é determinada pelo equilíbrio entre forças eletrostáticas e movimento térmico. Dessa forma, o potencial nessa região decai com o aumento da distância da superfície até que, a uma distância suficientemente grande, atinge o potencial da solução. Esse potencial é convencionado como potencial zero.
Em um campo elétrico, como em microeletroforese, cada partícula e os íons mais fortemente ligados à mesma se movem como uma unidade, e o potencial no plano de cisalhamento entre essa unidade e o meio circundante é chamada potencial zeta.
Quando uma camada de macromoléculas é adsorvida na superfície da partícula, ela move o plano de cisalhamento para longe da superfície e altera o potencial zeta.
Dessa forma, o potencial zeta é função da carga superficial da partícula, de qualquer camada adsorvida na interface com o meio e da natureza e composição do meio que a circunda.
Esse potencial pode ser determinado experimentalmente e, como ele reflete a carga efetiva nas partículas, ele se correlaciona com a repulsão eletrostática entre elas e com a estabilidade da suspensão.
Quando o potencial zeta é importante?
O potencial zeta é um indicador útil dessa carga e pode ser usado para prever e controlar a estabilidade de suspensões ou emulsões coloidais.
Quanto maior o potencial zeta mais provável que a suspensão seja estável pois as partículas carregadas se repelem umas às outras e essa força supera a tendência natural à agregação.
| Potencial zeta |ζ| em mV | Estabilidade da suspensão |
|---|---|
| 0 a 10 | coagulação ou floculação |
| 10 a 30 | pouca estabilidade |
| 30 a 40 | estabilidade moderada |
| 40 a 60 | boa estabilidade |
| > 60 | excelente estabilidade |
Essa é uma regra geral. Há exceções.
A medida do potencial zeta é com frequência a chave para compreender processos de dispersão e agregação em aplicações tão diversas quanto purificação de água, cerâmicas ou a formulação de tintas, fármacos e cosméticos.
Estabilidade Coloidal
- Sólidos têm energia livre mais baixa do que coloides e são estáveis enquanto que os coloides existem em um estado meta-estavel - eles estão constantemente sob a influência de forças atrativas.
- Forças repulsivas evitam a sua agregação.
- Na maioria dos líquidos polares essas forças são provenientes das cargas das partículas.
- Mudanças na energia livre podem provocar instabilidade do estado.
- A estabilidade pode ser ajustada e medida.
- O potential zeta é uma medida da estabilidade de uma dispersão.
- Potencial zeta mais elevado implica dispersão mais estavel.
- Valores baixos podem indicar instabilidade coloidal que pode levar à agregação.
- Contraíons se acumulam junto à superfície da partícula.
- Devido à difusão, os contraíons e co-íons eventualmente atingem o equilíbrio.
- No plano de cisalhamento, a diferença de potencial é definida como o potencial zeta.
- O potencial zeta depende da química da superfície, não da química volumetrica.
Ponto Isoelétrico
O potencial zeta muda com:
- Concentração de sais
- Concentração de íons que determinam o potencial, por exemplo, pH
- Concentração de surfactantes
A concentração do íon determinante do potencial na qual o potencial zeta é zero é definida como o ponto isoelétrico (PIE; IEP em inglês).
O ponto isoelétrico é uma medida muito importante e relaciona-se fortemente com a estabilidade.
Como medir o potencial zeta?
Não dispomos de pontas de prova infinitamente pequenas, nem teríamos como conectar essas pontas de prova à superfície de nossa nanopartícula em suspensão. Dessa forma, temos de usar alguma técnica indireta. A técnica mais usada é a mobilidade eletroforética.
Leia Mais...

 19 3289 9649
19 3289 9649